当前位置:首页 > 知识 > 欧盟委员会批准SKYRIZI®用于治疗成人活动性银屑病关节炎
内容介绍:2021年11月17日,艾伯维公司宣布,欧盟委员会(EC)已批准SKYRIZI(risankizumab)单药治疗或与甲氨蝶呤(methotrexate,MTX)联合使用,用于治疗对一种或多种抗风湿药物(DMARDs)反应不充分或不耐受的成人活动性银屑病关节炎。
2021年11月17日,艾伯维公司宣布,欧盟委员会(EC)已批准SKYRIZI®(risankizumab)单药治疗或与甲氨蝶呤(methotrexate,MTX)联合使用,用于治疗对一种或多种抗风湿药物(DMARDs)反应不充分或不耐受的成人活动性银屑病关节炎。这是SKYRIZI的第二个适应症,该市场授权将在欧盟所有成员国以及冰岛、列支敦士登、挪威和北爱尔兰有效。

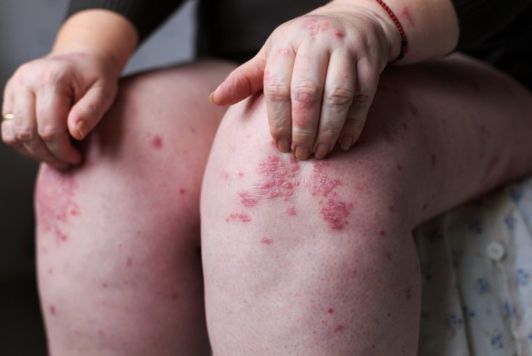
银屑病关节炎是一种异质性、系统性的炎症疾病,其特征性表现跨越多个领域,包括关节和皮肤。在银屑病关节炎中,免疫系统产生的炎症可导致疼痛、疲劳、关节僵硬和银屑病皮损的出现。
SKYRIZI是一种白细胞介素-23(IL-23)抑制剂,通过与IL-23的p19亚基结合而选择性地阻断IL-23。IL-23是一种参与炎症过程的细胞因子,与一些慢性免疫介导的疾病有关,包括银屑病。SKYRIZI的批准剂量为150毫克(可以是两支75毫克的预装注射器注射,也可以是一支150毫克的预装注射器注射),在第0周和第4周通过皮下注射给药,此后每12周一次。SKYRIZI 150毫克制剂于2021年5月获得欧盟批准。SKYRIZI在银屑病、克罗恩病、溃疡性结肠炎和银屑病关节炎中的3期试验正在进行。
该批准基于两项三期临床研究(KEEPsAKE-1和KEEPsAKE-2)的数据。在这些研究中,与安慰剂相比,SKYRIZI在第24周达到了ACR20反应的主要终点,并对次要终点进行了排名,包括但不限于银屑病关节炎几种临床表现的改善,如身体功能(通过健康评估问卷残疾指数[HAQ-DI]测量)第24周时的最低疾病活动度(MDA)。
艾伯维公司副董事长兼总裁、医学博士Michael Severino说:“我们很高兴欧盟可以批准SKYRIZI用于治疗成人活动性银屑病关节炎,银屑病关节炎患者会与银屑病皮损和关节炎症引起的肿胀和疼痛作斗争,减少这些症状可能使患者恢复正常生活并改善他们的生活质量。”




