当前位置:首页 > 知识 > 适用于所有斑块型银屑病成人患者,阿普斯特获FDA批准!
内容介绍:2021年12月20日,安进公司宣布,美国食品和药物管理局(FDA)已批准Otezla(apremilast,阿普斯特)用于治疗斑块型银屑病成人患者(适合光疗或系统治疗)。随着适应症的扩大,Otezla成为首个也是唯一一个被批准用于所有严重程度(包括轻度、中度和重度)的斑块型银屑病成人患者的口服药物。
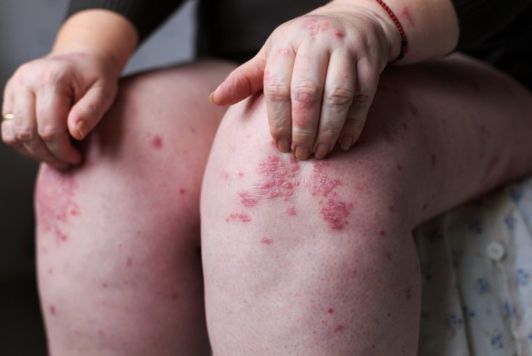
银屑病是一种严重的慢性炎症性疾病。在美国,大约有800万人患有斑块型银屑病,500万人患有轻度至中度疾病。近年来,尽管斑块型银屑病的治疗取得了进展,但仍有大量需求尚未得到满足,特别是轻度至中度斑块型银屑病患者或既往接受过局部治疗但仍有持续症状的患者。
2021年12月20日,安进公司宣布,美国食品和药物管理局(FDA)已批准Otezla (apremilast,阿普斯特)用于治疗斑块型银屑病成人患者(适合光疗或系统治疗)。随着适应症的扩大,Otezla成为首个也是唯一一个被批准用于所有严重程度(包括轻度、中度和重度)的斑块型银屑病成人患者的口服药物。

美国国家银屑病基金会首席医疗官Stacie Bell博士说:“斑块型银屑病对患者的影响通常比仅用体表面积来衡量的还要严重,特别是那些在头皮等难以治疗的区域有表现的患者。斑块的位置会影响局部治疗的敏感度和难易程度。值得高兴的是,终于有一种可供选择且具有良好的安全性的口服药物,适用于所有斑块型银屑病成人患者。”
FDA的批准是基于3期ADVANCE试验的数据,在轻度至中度斑块型银屑病成人患者中,第16周时,Otezla组(剂量为30mg,每日两次)达到静态医师全球评估(sPGA)反应的主要终点的患者是安慰剂组的5倍(21.6% vs. 4.1%),这一差异具有统计学显著性。另外,与安慰剂相比,第16周时,Otezla在关键症状方面也有显著改善,如全身瘙痒NRS反应(43.2% vs 18.6%),以及根据头皮医师全球评估(ScPGA)反应测量的难以治疗的头皮区域(44% vs 16.6%)。早在第2周就观察到sPGA反应、全身瘙痒NRS反应和ScPGA反应的改善,并一直维持到第32周。
该试验中观察到的不良事件与Otezla已知的安全性一致。最常见的治疗紧急不良事件(≥5%)为腹泻、头痛、恶心和鼻咽炎。
在美国,Otezla已经获批3种适应症,包括适合光疗或系统治疗的斑块型银屑病成人患者、活动性银屑病关节炎成人患者以及Behçet病相关口腔溃疡的成人患者。Otezla是斑块型银屑病患者开始系统治疗时最常用的处方品牌。安进公司还致力于研究Otezla在整个银屑病连续过程中的潜力,包括生殖器型银屑病、儿童银屑病、青少年银屑病关节炎等。




